от профессора Аверьянова
Дышится легче
Авторы: А.В. Аверьянов1, О.И. Балионис1, В.Н. Лесняк2
1 Научно-исследовательский институт пульмонологии ФМБА России, Москва
2 Федеральный научно-клинический центр специализированных видов медицинской помощи и медицинских технологий ФМБА России, Москва
Резюме
Саркоидоз — гранулематозное заболевание неустановленной этиологии, при котором в патологический процесс вовлекаются различные органы и ткани. Изменения в легких, медиастинальных и внутригрудных лимфатических узлах встречаются у 90% больных саркоидозом. Рентгенологические проявления саркоидоза легких характеризуются значительной вариабельностью. В статье описаны атипичные компьютерно-томографические (КТ) находки, мимикрирующие под другие болезни легких, такие как опухолевидные инфильтраты, «матовое стекло», ретикулярные изменения, полости, плевральный выпот. Также даны описания очаговых и ретикулонодулярных изменений (изолированные ретикулярные изменения за счет утолщения внутри- и междольковых перегородок наблюдаются примерно у 50% больных саркоидозом, но являются преобладающим КТ-паттерном только у 15–20% больных), зон консолидации, фиброзных изменений. Как правило, саркоидные изменения в паренхиме легких сочетаются с внутригрудной лимфаденопатией, которая встречается у 80% пациентов с саркоидозом. В большинстве случаев изменения носят двусторонний характер. У 10–13% пациентов определяются крупные очаги (8–12 мм в диаметре) однородной структуры с четкими контурами, располагающиеся преимущественно вдоль листков костальной и междолевой плевры, в междольковых перегородках, напоминающих метастатические очаги. У 2,4–4% больных мелкие, типичные для саркоидоза очаги могут отсутствовать, а изменения представлены более крупными узловыми образованиями (>2 см в диаметре) или массами с неровными контурами. Саркоидоз, имитирующий интерстициальную пневмонию, чаще проявляется симптомом «матового стекла», имеющим обычно пятнистую форму, преимущественно в верхних отделах легких. Этот признак встречается у 16–83% пациентов с саркоидозом, чаще в дебюте заболевания и обычно сочетается с очаговыми изменениями в легких и внутригрудной лимфаденопатией. Описаны полостные формы саркоидоза легких.
Ключевые слова: саркоидоз, КТ, компьютерная томография, атипичные проявления.
Введение
Саркоидоз — это мультисистемное гранулематозное заболевание неустановленной этиологии, характеризующееся образованием неказеозных гранулем с вовлечением в патологический процесс различных органов [1]. Изменения в легких, медиастинальных и внутригрудных лимфатических узлах встречаются у 90% больных саркоидозом [2, 3]. В соответствии с последним консенсусом Американского торакального общества (2020), диагноз саркоидоза легких устанавливается на основании сочетания характерной клинической и рентгенологической картины, признаков гранулематозного воспаления, подтвержденных гистологически, при исключении альтернативных гранулематозных процессов [4]. Рентгенологические, выявляемые на компьютерной томографии высокого разрешения (КТВР), проявления саркоидоза легких характеризуются значительной вариабельностью. Его типичные проявления представлены ниже.
У 90% больных саркоидозом при вовлечении в процесс легочной паренхимы встречаются очаговые изменения в легких [5]. Очаги, как правило, мелкие (2–4 мм в диаметре), четко очерченные, располагаются симметрично, преимущественно в верхних и средних отделах легких. При саркоидозе чаще наблюдается перилимфатическое распределение очагов, при котором изменения располагаются преимущественно вдоль бронхососудистых пучков, междольковых перегородок и субплеврально, что создает картину неровных контуров анатомических структур и четко-образного утолщения перегородок и стенок сосудов и бронхов (рис. 1).
Изолированные ретикулярные изменения за счет утолщения внутри- и междольковых перегородок наблюдаются примерно у 50% больных саркоидозом, но являются преобладающим КТ-паттерном только у 15–20% больных. Изменения чаще субплевральные, превалируют в верхних и средних отделах легких [2].
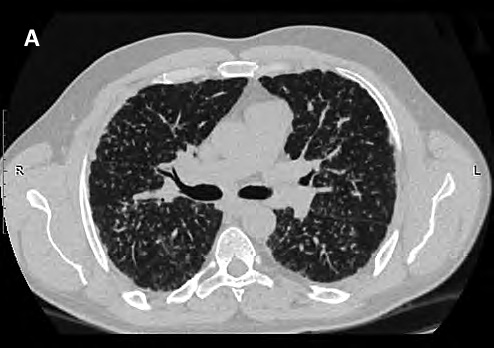
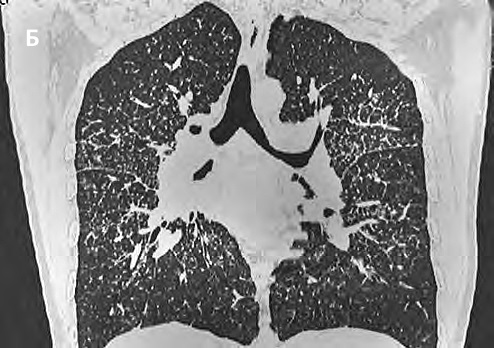
Рис. 1. Характерные КТ-проявления легочного саркоидоза: А — множественные мелкие очаги, имеющие перилимфатическое распределение, местами сливающиеся между собой. Прилежание очагов к перибронховаскулярному интерстицию создает картину неравномерного, четкообразного его утолщения. Присутствие большого количества узелков на листках костальной и междолевой плевры придает им мелкобугристый вид. В прикорневых зонах видны пакеты увеличенных лимфатических узлов; Б — наиболее выраженные изменения при типичных проявлениях саркоидоза регистрируются в верхних и средних долях, сегментах язычка верхней доли левого легкого, что наилучшим образом отображается на мультипланарных, особенно фронтальных, реконструкциях
Альвеолярные инфильтраты встречаются у 10– 20% больных саркоидозом [6–8], изменения обычно симметричные, двусторонние, локализуются преимущественно в верхних и средних отделах легких. В зонах инфильтрации часто прослеживается симптом воздушной бронхографии (рис. 2).
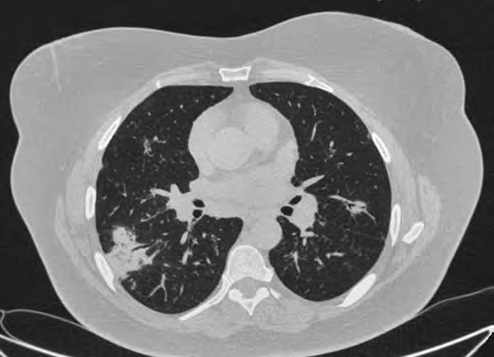
Рис. 2. Альвеолярная форма легочного саркоидоза. В периферических отделах S6 нижней доли правого легкого выявляется средних размеров зона консолидации, захватывающая кортикальный
и субкортикальный слои, имеющая крупнобугристые очертания, в структуре которого прослеживаются воздушная полоска бронха и точечные скопления воздуха в бронхиолах. Инфильтрат небольших размеров регистрируется также в верхней доле левого
легкого, сливной очаг — в верхней доле правого легкого. С обеих сторон, больше в S6 левого легкого, — множественные мелкие перилимфатические очаги. Умеренное расширение корней легких за счет увеличения лимфатических узлов
Фиброзные изменения описывают у 10–20% больных саркоидозом легких, они формируются, как правило, при длительном течении заболевания [9]. Подобные изменения представлены фиброзными пучками, подтягиванием корней, тракционными бронхоэктазами, симптомом «сотового легкого», неравномерным утолщением междольковых и внутридольковых перегородок. Изменения максимально выражены в верхних и средних отделах легких (рис. 3).
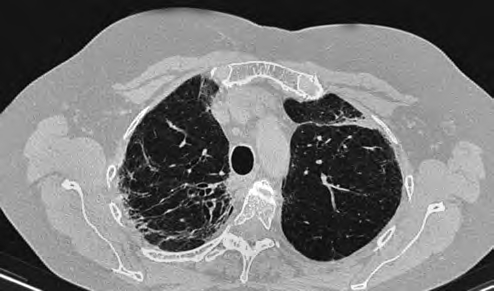
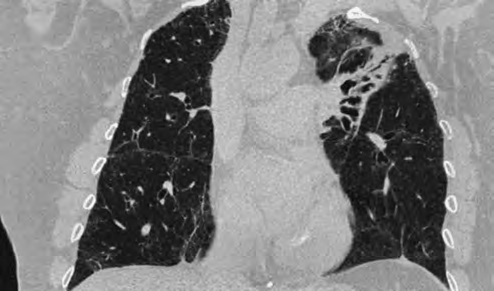
Рис. 3. Фиброзная форма саркоидоза легких. Легкие эмфизематозны на всем протяжении за счет распространенной парасептальной эмфиземы с наличием междолькового линейного фиброза. Нарушение архитектуры верхних долей легких с их объемным уменьшением из-за выраженного фиброза, сопровождающегося грубым расширением бронхов по типу тракционных бронхо- и бронхиолоэктазов. Утолщение апикальной плевры слева
В 60% случаев формирования фиброза при саркоидозе вокруг сосудов и бронхов формируются участки консолидации и конгломераты, вызывающие смещение бронхов верхних долей кзади, уменьшение объема задних сегментов верхних долей [6]. Кисты, тракционные бронхоэктазы и парафиброзная эмфизема встречаются только при далеко зашедших стадиях саркоидоза. Кистозные изменения в большей степени выражены в верхних долях легких. «Сотовое легкое» при саркоидозе встречается реже, чем при других фиброзирующих интерстициальных заболеваниях; изменения в большей степени выражены в верхних долях легких, однако и нижние доли тоже могут быть вовлечены в патологический процесс, что может напоминать картину идиопатического легочного фиброза (ИЛФ) [10].
Как правило, саркоидные изменения в паренхиме легких сочетаются с внутригрудной лимфаденопатией, которая встречается у 80% пациентов с саркоидозом. В большинстве случаев изменения носят двусторонний характер [11, 12]. Чаще всего имеет место увеличение лимфатических узлов корней легких, правой паратрахеальной, трахеобронхиальной групп и лимфоузлов аортопульмонального окна [11]. Увеличение лимфатических узлов корней легких и правой паратрахеальной группы известно как «триада Гарланда». Лимфатические узлы обычно множественные, имеют вид псевдоконгломератных образований, однородной структуры, с четкими контурами, без зон некроза, могут содержать кальцинаты (последние встречаются при длительном течении заболевания) (рис. 4).
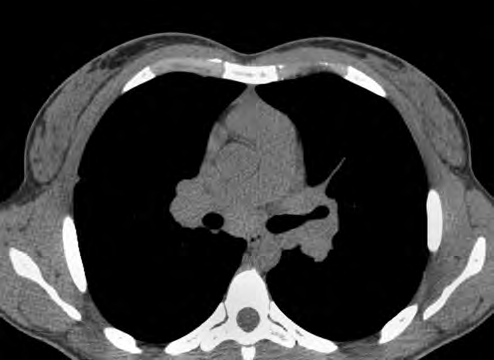
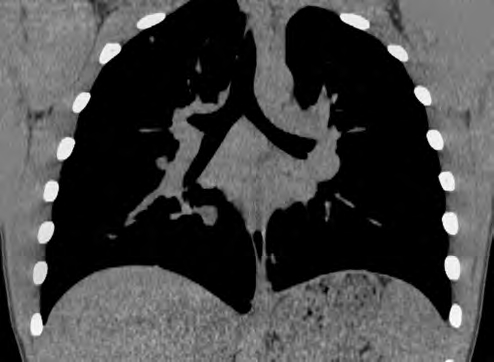
Рис. 4. Внутригрудная лимфаденопатия при саркоидозе. Увеличение всех групп внутригрудных лимфатических узлов и узлов бронхиальных групп с образованием псевдоконгломерата
В случаях описанных выше находок на КТВР у рентгенолога и клинициста обычно не возникает затруднений в трактовке диагноза, особенно если это сочетается с другими признаками саркоидоза (синдром Лефгрена, узловатая эритема, синдром Хеерфордта, lupus pernio, гиперкальциурия и/или гиперкальцемия c повышением уровня витамина D) и часто не требует морфологической верификации [4]. Однако у некоторых пациентов типичные КТ-признаки саркоидоза легких отсутствуют, а представленные изменения могут мимикрировать под другие заболевания. В целом такие пациенты составляют примерно 15% больных саркоидозом легких [13]. Именно эти атипичные КТ-проявления, с которых может манифестировать саркоидоз, мы хотели бы рассмотреть более подробно, основываясь на опыте работы более чем с 150 больными с морфологически подтвержденным диагнозом.
Появление очаговых образований в легких всегда включает в дифференциальный ряд опухолевые процессы. У 10–13% пациентов определяются крупные очаги (8–12 мм в диаметре) однородной структуры с четкими контурами, располагающиеся преимущественно вдоль листков костальной и междолевой плевры, в междольковых перегородках, напоминающих метастатические очаги [14]. У 2,4–4% больных мелкие, типичные для саркоидоза очаги могут отсутствовать, а изменения представлены более крупными узловыми образованиями (>2 см в диаметре) или массами с неровными контурами [15, 16]. Подобные изменения чаще носят двусторонний характер и располагаются ближе к периферии [17], в редких случаях характеризуются формированием полостей [18, 19]. Если у пациента имеется предшествующий опухолевый анамнез, такие признаки трактуются обычно как метастатический процесс с последующим назначением химиотерапии без морфологической верификации диагноза. Еще более сложной является ситуация, когда у больного имеется активный опухолевый процесс, проводится терапия иммуномодулирующими препаратами (в особенности ингибиторами контрольных точек иммунного ответа) и в легких развивается саркоидная гранулематозная реакция на опухоль или лекарство. Тогда даже типичный для саркоидоза легких КТ-паттерн, как правило, расценивается как вторичные опухолевые изменения. Между тем, для метастазов в легкие характерны следующие признаки [20]:
В целом очаги размером менее 5 мм в большинстве случаев имеют доброкачественный характер, с увеличением их размеров вероятность их злокачественного генеза существенно возрастает [21]. Саркоидные очаги, если они локализуются в нижних отделах легких и имеют размеры более 5 мм, практически неотличимы по остальным признакам от метастатического процесса (рис. 5). Помощь в дифференциальной диагностике в таких случаях может оказать ПЭТ-КТ, поскольку метаболизм и накопление радиоактивной фтордезоксиглюкозы в таких образованиях существенно ниже, чем в опухолевых узлах.
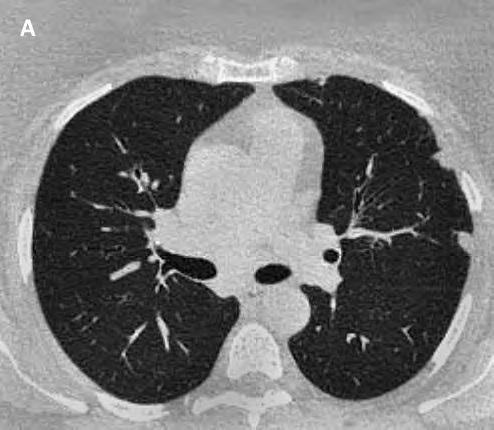
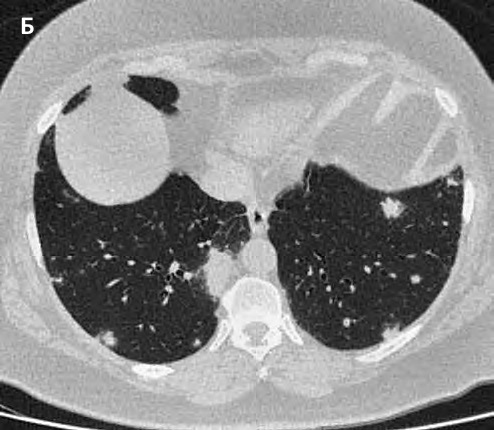
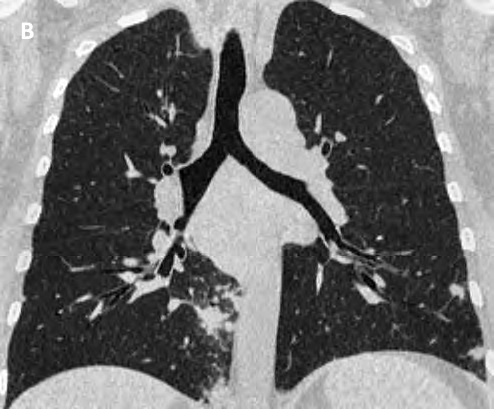
Рис. 5. Псевдоопухолевое поражение паренхимы легких при саркоидозе: А, Б — многочисленные крупные очаги неправильно округлой формы с лучистыми очертаниями, локализующиеся преимущественно в кортикальных отделах нижних долей; В — два крупных сливных очага с нечеткими очертаниями, окруженные многочисленными мелкими перилимфатическими очажками в S10 нижней доли правого легкого. Увеличение лимфатических узлов корней легких. Реконструкция в коронарной проекции
Наиболее редкими и особенно трудными в диагностике бывают узловые локальные формы саркоидоза легких либо одиночные конгломераты лимфатических узлов, мимикрирующие опухоль (рис. 6). Если при этом развивается обтурационный ателектаз, то даже гистологическое присутствие саркоидных гранулем в биопсийном материале может не остановить хирургов в попытке оперативного решения проблемы, поскольку КТ-картина кажется слишком характерной для опухолевого процесса.
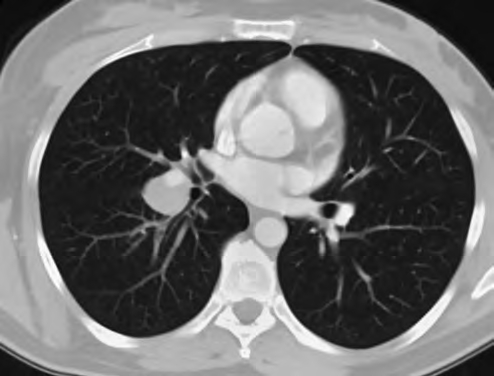
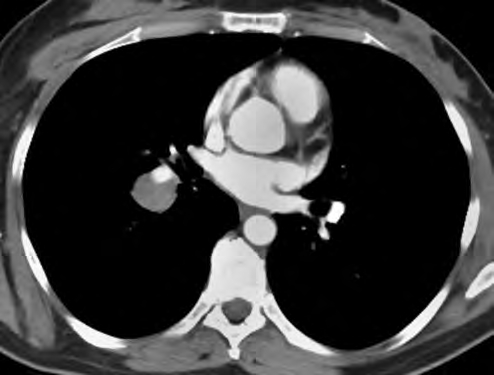
Рис. 6. Редкий вариант одностороннего поражения лимфатических узлов бронхопульмональной группы при саркоидозе. КТ с контрастированием. Крупный узел в области тела корня правого легкого, почти полностью охватывающий нижнедолевую ветвь легочной артерии, без признаков инвазии (А, Б)
Саркоидоз, имитирующий интерстициальную пневмонию, чаще проявляется симптомом «матового стекла», имеющим обычно пятнистую форму, преимущественно в верхних отделах легких. Данный признак встречается у 16–83% пациентов с саркоидозом [8, 22–24], чаще в дебюте заболевания [25] и обычно сочетается с очаговыми изменениями в легких и внутригрудной лимфаденопатией. В этих случаях заподозрить саркоидоз не представляет особых сложностей. Однако если «матовое стекло» является единственным или доминирующим КТ-признаком болезни, проблема дифференциальной диагностики с интерстициальными пневмониями, становится весьма актуальной (рис. 7). Ранее считалось, что формирование данного радиологического феномена обусловлено активным альвеолитом. В настоящее время полагают, что в его основе лежат множество мельчайших очагов и фиброзные изменения, находящиеся за пределами разрешающей способности КТ и неразличимые по отдельности [26]. Обычно одновременно присутствует несколько фокусов «матового стекла» [27].

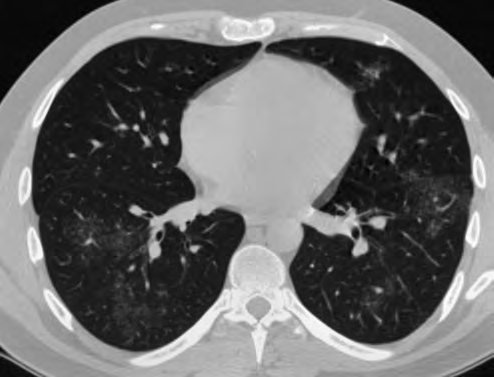
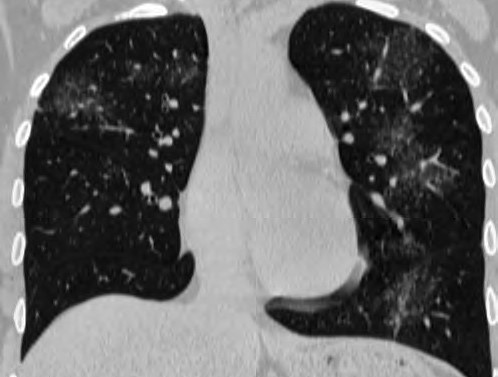
Рис. 7. Сакроидоз, мимикрирующий интерстициальную пневмонию. Достаточно обширные зоны «матового стекла» в сочетании с нежным мелкоочаговым поражением и ретикулярными изменениями, представленными преимущественно утолщением внутридолькового интерстиция
Еще одним КТ-симптомом, который может направить мысль врача в сторону несаркоидного интерстициального заболевания легких, является утолщение междольковых и внутридольковых перегородок (ретикулярный паттерн). В целом ретикулярные изменения наблюдаются примерно у 50% больных саркоидозом, но преобладают только у 15–20% больных. Изменения чаще субплевральные, превалируют в верхних и средних отделах легких [2]. Однако встречаются и диффузные ретикулярные изменения. Если другие радиологические признаки саркоидоза легких минимальны или отсутствуют, то утолщение внутри- и междольковых перегородок, особенно в сочетании с «матовым стеклом», часто расценивается как признак интерстициальной пневмонии (пневмонита) (рис. 8, 9).
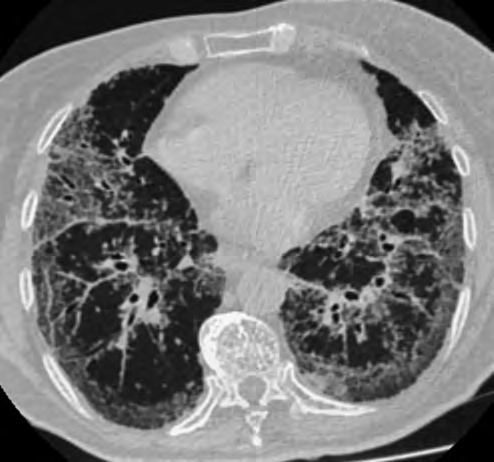
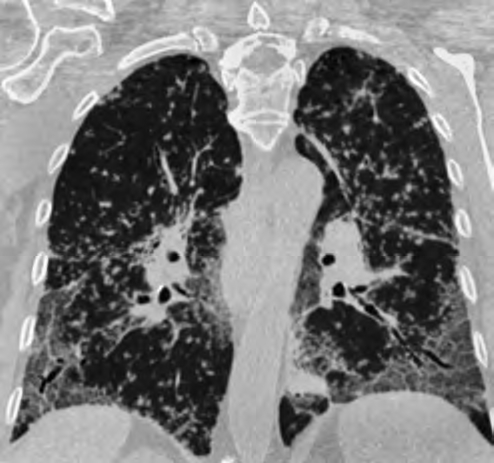
Рис. 8. Редкий вариант диффузного интерстициального поражения легких при саркоидозе. Множественные участки сливных ретикулярных изменений на фоне обширных зон матового стекла с тракционными бронхоэктазами с преимущественно заднебазальным распределением, напоминающие хроническую фиброзирующую интерстициальную пневмонию. Множественные мелкие плотные очажки с перилимфатическим распределением, образующие участки интенсивного матового стекла, тяготеющие к бронхососудистым пучкам и плащевому слою нижних долей, увеличение бронхопульмональных лимфатических узлов
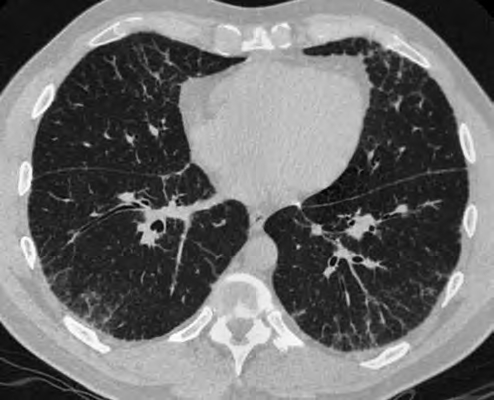
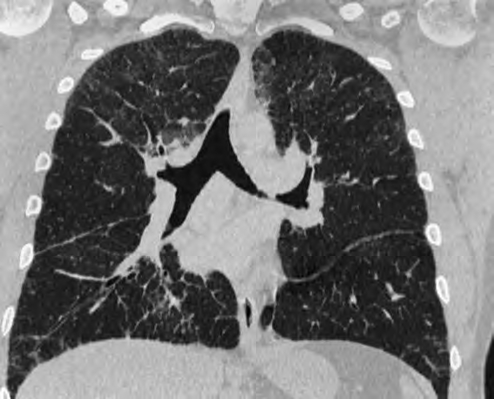
Рис. 9. Преобладающие ретикулярные изменения при саркоидозе легких. В КТ-картине доминирует ретикулярный паттерн в виде утолщения внутридольковых и междольковых перегородок как в верхних, так и нижних отделах легких. В корональной реконструкции также заметны разлитые зоны «матового стекла» в верхних долях
Формирование кистозных или буллезных полостей встречается примерно у 10% пациентов в терминальной стадии заболевания (рис. 10) [28]. Стенки таких полостей выстланы плотной фиброзной тканью [29]. Более редким (менее чем у 0,8% больных саркоидозом) является образование первичных полостей за счет центрального некроза [30], обычно среди молодых пациентов [31]. Стенки таких полостей выстланы сливающимися между собой гранулемами. В этих случаях необходимо проводить дифференциальную диагностику с фиброзно-кавернозным туберкулезом легких, а также думать о присоединении грибковой инфекции и формировании мицетом, которые имеют место примерно у 1–3% больных саркоидозом, как правило, при IV рентгенологической стадии саркоидного процесса [32]. Образование мицетом происходит за счет колонизации существующих булл и кист (обычно верхнедолевой локализации) сапрофитными грибами, чаще рода Aspergillus. Классическим КТ-симптомом аспергилломы является «симптом погремушки», представляющий собой внутриполостной фокус затемнения за счет мицелия гриба [33]. Появлению мицетомы обычно предшествует утолщение плевры рядом с известной ранее полостью. Общим симптомом у пациентов с аспрегилломами является кровохарканье и редко легочное кровотечение; последнее редко может носить жизнеугрожающий характер. Подобное осложнение является второй по частоте причиной смерти среди пациентов с саркоидозом легких [34].
При саркоидозе гранулематозный процесс может развиваться и в листках париетальной и висцеральной плевры, что наряду с блокадой гранулемами путей лимфатического оттока на уровне плевры и междольковых перегородок может приводить к развитию плеврального выпота. Плевральный выпот представляет собой редкое проявление саркоидоза и всегда требует рассмотрения возможной манифестации других заболеваний. В исследовании J.T. Huggins и соавт. из 181 больного саркоидозом с гидротораксом только у 1,1% выпот был связан с развитием саркоидного процесса в плевре, что было подтверждено результатами биопсии [35]. Плевральный выпот может быть экссудатом и транссудатом, чаще правосторонней локализации [36]. Плевральный выпот при саркоидозе, как правило, минимальный, разрешается самостоятельно в течение 6 мес. [10], иногда оставляя после себя остаточные плевральные утолщения [37, 38], однако может быть клинически значимым и рецидивирующим. В литературе встречается описание отдельных случаев развития хилоторакса и эозинофильного экссудата при саркоидозе [39–42].
При саркоидозе, как правило, имеет место двустороннее относительно симметричное увеличение внутригрудных лимфоузлов. Односторонние (чаще правосторонние) изменения описаны в 3–5% случаев [37, 43]. Еще реже встречается изолированное увеличение медиастинальных лимфоузлов без увеличения лимфоузлов корней легких [28, 44]. Асимметричное, одностороннее поражение внутригрудных лимфатических узлов, а также вовлечение в патологический процесс необычных групп лимфоузлов чаще встречается у пациентов старше 50 лет [7]. Такие случаи всегда требуют дифференциальной диагностики с онкологическим заболеванием. Довольно часто односторонняя лимфаденопатия встречается лишь в дебюте заболевания и по мере развития болезни становится двусторонней [45].
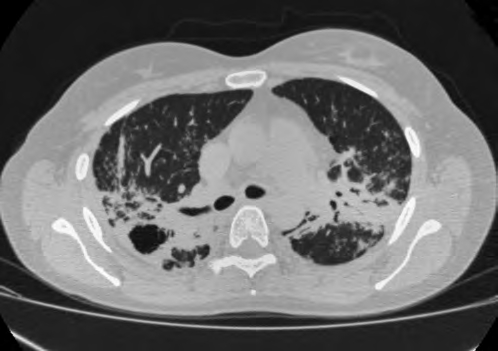
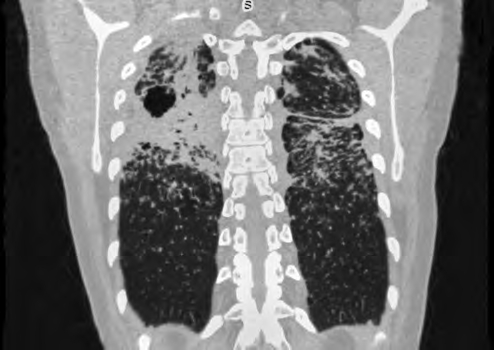
Рис. 10. Полостная форма саркоидоза легких. В верхней доле правого легкого — выраженные инфильтративные изменения сливного характера с наличием полости распада, содержащей воздух. В левом легком — зоны консолидации, а также уплотнение легочной ткани вблизи междолевой плевры. Практически во всех отделах регистрируются многочисленные перилимфатические очаги с нечеткими контурами, местами — с тенденцией к слиянию. Утолщена плевра соответственно локализации инфильтративных изменений
Существует еще ряд радиологических феноменов, редко встречающихся при саркоидозе легких. Например, симптом «галактики», представляющий собой крупный фокус консолидации, окруженный маленькими сателлитными очагами [46]; симптом «кластера», характеризующийся скоплением большого количества мелких очагов, формирующих более крупный очаг, но без слияния в центре [47], симптомы «гало» и «обратного гало» [48, 49]. Также довольно редкие, но возможные КТ-проявления саркоидоза легких — симптомы «мозаичной плотности» и «воздушных ловушек» за счет неравномерной вентиляции и перфузии легочной паренхимы из-за обструкции мелких воздухоносных путей саркоидными гранулемами. Тем не менее все они не встречаются изолированно от типичных КТ-изменений и поэтому не рассматриваются в данной статье.
Проявления саркоидоза легких на КТВР многообразны и изменчивы. Тем не менее можно выделить ряд типичных и атипичных проявлений заболевания. Первые позволяют заподозрить диагноз, который в дальнейшем обычно подтверждается клинически, лабораторно или морфологически. Атипичные радиологические формы саркоидоза легких чаще всего мимикрируют другие заболевания легких и требуют применения инвазивных методов диагностики, а порой и полостных хирургических вмешательств. Однако знание пульмонологами, торакальными хирургами и рентгенологами редких КТ-манифестаций саркоидоза легких может помочь в таких случаях использовать малоинвазивные технологии, такие как трансбронхиальная биопсия легких, эндобронхиальная пункция ВГЛУ под контролем эндо-УЗИ или ПЭТ-КТ, часто позволяющие установить правильный диагноз более щадящими способами.
1. Чучалин А.Г., Авдеев С.Н., Айсанов З.Р. и др. Федеральные клинические рекомендации Российского респираторного общества по диагностике и лечению саркоидоза. Пульмонология 2019; 1–47 [Chuchalin A.G., Avdeev S.N., Ajsanov Z.R. et al. Federal clinical guidelines of the Russian Respiratory Society for the diagnosis and treatment of sarcoidosis. Pul’monologija 2019; 1–47 (In Russ.)].
2. Criado E., Sanchez M., Ramirez J., Arguis P., de Ca ralt T.M., Perea R.J., Xaubet A. Pulmonary sarcoidosis: typical and atypical manifestations at high-resolution CT with pathologic correlation. Radiographics 2010; 30 (6): 1567–1586.
3. Statement on sarcoidosis. Joint Statement of the American Thoracic Society (ATS), the European Respiratory Society (ERS) and the World Association of Sarcoidosis and Other Granulomatous Disorders (WASOG) adopted by the ATS Board of Directors and by the ERS Executive Committee, February 1999. Am. J. Respir. Crit. Care Med. 1999; 160: 736–755.
4. Crouser E.D., Maier L.A., Wilson K.C. et al. Diagnosis and Detection of Sarcoidosis. An Official American Thoracic Society Clinical Practice Guideline. Am. J. Respir. Crit. Care Med. 2020 Apr 15; 201 (8): e26-e51.
5. McLoud T.C., Epler G.R., Gaensler E.A., Burke G.W., Carrington C.B. A radiographic classification for sarcoidosis: physiologic correlation. Invest Radiol. 1982; 17 (2): 129–138.
6. Abehsera M., Valeyre D., Grenier P., Jaillet H., Battesti J.P., Brauner M.W. Sarcoidosis with pulmonary fibrosis: CT patterns and correlation with pulmonary function. AJR Am J. Roentgenol. 2000; 174 (6): 1751–1757.
7. Conant E.F., Glickstein M.F., Mahar P., Miller W.T. Pulmonary sarcoidosis in the older patient: conventional radiographic features. Radiology 1988; 169 (2): 315–319.
8. Remy-Jardin M., Giraud F., Remy J., Wattinne L., Wallaert B., Duhamel A. Pulmonary sarcoidosis: role of CT in the evaluation of disease activity and functional impairment and in prognosis assessment. Radiology 1994; 191 (3): 675–680.
9. Moller D.R. Pulmonary fibrosis of sarcoidosis. New approaches, old ideas. Am. J. Respir Cell Mol. Biol. 2003; 29 (3): 37–41.
10. Padley S.P., Padhani A.R., Nicholson A., Hansell D.M. Pulmonary sarcoidosis mimicking cryptogenic fibrosingalveolitis on CT. Clin. Radiol. 1996; 51 (11): 807–810.
11. Patil S.N., Levin D.L. Distribution of thoracic lymphadenopathy in sarcoidosis using computed tomography. J. Thorac Imaging 1999; 14 (2): 114–117.
12. Sider L., Horton Jr E.S. Hilar and mediastinaladenopathy in sarcoidosis as detected by computed tomography. J. Thorac Imaging 1990; 5 (2): 77–80.
13. Dhagat P.K., Singh S., Jain M., Singh S.N., Sharma R.K. Thoracic Sarcoidosis: Imaging with High Resolution Computed Tomography. J. Clin. Diagn. Res. 2017; 11 (2): TC15-TC18.
14. Gotway M.B., Tchao N.K., Leung J.W., Hanks D.K., Thomas A.N. Sarcoidosis presenting as an enlarging solitary pulmonary nodule. J. Thorac Imaging 2001; 16 (2): 117–122.
15. Kirks D.R., McCormick V.D., Greenspan R.H. Pulmonary sarcoidosis. Roentgenologic analysis of 150 patients. Am. J. Roentgenol Radium Ther. Nucl. Med. 1973; 117 (4): 777–786.
16. Sharma O.P., Hewlett R., Gordonson J. Nodular sarcoidosis: an unusual radiographic appearance. Chest. 1973; 64 (2): 189–192.
17. Battesti J.P., Saumon G., Valeyre D., Amouroux J., Pechnick B., Sandron D. et al. Pulmonary sarcoidosis with an alveolar radiographic pattern. Thorax 1982; 37 (6): 448–452.
18. Edelman R.R., Johnson T.S., Jhaveri H.S., Kim D., Kasdon E., Frank H.A. et al. Fatal hemoptysis resulting from erosion of a pulmonary artery in cavitarysarcoidosis. AJR Am J. Roentgenol. 1985; 145 (1): 37–38.
19. Loh G.A., Lettieri C.J., Shah A.A. Bronchial arterial embolisation for massive haemoptysis in cavitarysarcoidosis. BMJ Case Rep. 2013.
20. Difficult to Diagnose Rare Diffuse Lung Disease. 1st Edition (ed. Alexander Averyanov). Elsevier Academic Press. ISBN 9780128153758. 2020; 383–391.
21. Murata K., Takahashi M., Mori M. et al.Pulmonary metastatic nodules: CT-pathologic correlation. Radiology 1992; 182 (2): 331–335.
22. Grenier P., Chevret S., Beigelman C., Brauner M.W., Chastang C., Valeyre D. Chronic diffuse infiltrative lung disease: determination of the diagnostic value of clinical data, chest radiography, and CT and Bayesian analysis. Radiology 1994; 191 (2): 383–390.
23. Grenier P., Valeyre D., Cluzel P., Brauner M.W., Lenoir S., Chastang C. Chronic diffuse interstitial lung disease: diagnostic value of chest radiography and high-resolution CT. Radiology 1991;179 (1): 123–132.
24. Leung A.N., Brauner M.W., Caillat-Vigneron N., Valeyre D., Grenier P. Sarcoidosis activity: correlation of HRCT findings with those of 67 Ga scanning, bronchoalveolar lavage, and serum angiotensin-converting enzyme assay. J. Comput Assist Tomogr. 1998; 22 (2): 229–234.
25. Brauner M.W., Grenier P., Mompoint D., Lenoir S., de Cremoux H. Pulmonary sarcoidosis: evaluation with high-resolution CT. Radiology 1989; 172 (2): 467–471.
26. Ma C., Zhao Y., Wu T. Predominant diffuse ground glass opacity in both lung fields: a case of sarcoidosis with atypical CT findings. Respir. Med. Case Rep. 2016; 17: 61–63.
27. Martin S.G., Kronek L.P., Valeyre D., Brauner N., Brillet P.Y., Nunes H. et al. High-resolution computed tomography to differentiate chronic diffuse interstitial lung diseases with predominant ground-glass pattern using logical analysis of data. Eur. Radiol. 2010; 20 (6): 1297–1310.
28. Rockoff S.D., Rohatgi P.K. Unusual manifestations of thoracic sarcoidosis. AJR Am. J. Roentgenol. 1985; 144 (3): 513–528.
29. Ichikawa Y., Fujimoto K., Shiraishi T., Oizumi K. Primary cavitarysarcoidosis: high-resolution CT findings. AJR Am. J. Roentgenol 1994; 163 (3): 745.
30. Mayock R.L., Bertrand P., Morrison C.E., Scott J.H. Manifestations of sarcoidosis: analysis of 145 patients, with a review of nine series selected from the literature. Am. J. Med. 1963; 35: 67–89.
31. Rohatgi P.K., Schwab L.E. Primary acute pulmonary cavitation in sarcoidosis. AJR Am. J. Roentgenol. 1980; 134 (6): 1199–1203.
32. Pena T.A., Soubani A.O., Samavati L. Aspergillus lung disease in patients with sarcoidosis: a case series and review of the literature. Lung 2011; 189 (2): 167–172.
33. Pesle G.D., Monod O. Bronchiectasis due to asperigilloma. Dis Chest 1954; 25 (2): 172–183.
34. Israel H.L., Lenchner G.S., Atkinson G.W. Sarcoidosis and aspergilloma: the role of surgery. Chest 1982; 82 (4): 430–432.
35. Huggins J.T., Doelken P., Sahn S.A., King L., Judson M.A.Pleural effusions in a series of 181 outpatients with sarcoidosis. Chest 2006; 129 (6): 1599–1604.
36. Soskel N.T., Sharma O.P. Pleural involvement in sarcoidosis. Curr. Opin. Pulm. Med. 2000; 6 (5): 455–468.
37. Rabinowitz J.G., Ulreich S., Soriano C. The usual unusual manifestations of sarcoidosis and the “hilar haze” — a new diagnostic aid. Am. J. Roentgenol. Radium Ther. Nucl. Med. 1974; 120 (4): 821–823.
38. Wilen S.B., Rabinowitz J.G., Ulreich S., Lyons H.A.Pleural involvement in sarcoidosis. Am. J. Med. 1974; 57 (2): 200–209.
39. Aberg H., Bah M., Waters A.W. Sarcoidosis: complicated by chylothorax. Minn Med. 1966; 49 (7): 1065–1070.
40. Jarman P.R., Whyte M.K., Sabroe I., Hughes J.M. Sarcoidosis presenting with chylothorax. Thorax 1995; 50 (12): 1324–1325.
41. Lengyel R.J., Shanley D.J. Recurrent chylothorax associated with sarcoidosis. Hawaii Med. J. 1995; 54 (12): 817–818.
42. Vafiadis E., Sidiropoulou M.S., Voutsas V., Giannopoulos T.L., Iordanidis F., Christaki P. et al. Eosinophilic pleural effusion, peripheral eosinophilia, pleural thickening, and hepatosplenomegaly in sarcoidosis. South Med. J. 2005; 98: 1218–1222.
43. Romer F.K. Presentation of sarcoidosis and outcome of pulmonary changes. Dan. Med. Bull. 1982; 29 (1): 27–32.
44. Hamper U.M., Fishman E.K., Khouri N.F., Johns C.J., Wang K.P., Siegelman S.S. Typical and atypical CT manifestations of pulmonary sarcoidosis. J. Comput Assist Tomogr. 1986; 10 (6): 928–936.
45. Al-Jahdali H., Rajiah P., Koteyar S.S., Allen C., Khan A.N. Atypical radiological manifestations of thoracic sarcoidosis: A review and pictorial essay. Ann. Thorac. Med. 2013; 8: 186–196.
46. Nakatsu M., Hatabu H., Morikawa K. et al. Large coalescent parenchymal nodules in pulmonary sarcoidosis: “sarcoid galaxy” sign. AJR Am J. Roentgenol. 2002; 178 (6): 1389–1393.
47. Ortega Н.I., Orcajo А.N., González L.L. The “sarcoid cluster sign”: a new sign in high resolution chest CТ. Radiologia 2009; 51 (5): 495–499.
48. Marchiori E., Zanetti G., Duarte Guimarães M., Hochhegger B. The reversed halo sign extending the spectrum of atypical radiological manifestations in sarcoidosis. Ann. Thorac. Med. 2014; 9 (1): 48.
49. Marten K., Rummeny E.J., Engelke C. The CT halo: a new sign in active pulmonary sarcoidosis. J. Radiol. 2004; 77: 1042–1045.
При цитировании или копировании статей гиперссылка на сайт https://profaveryanov.com обязательна!